近日,武汉大学生命科学学院/泰康生命医学中心宋保亮团队在EMBO Journal 发表了题为GRAMD1/ASTER-mediated cholesterol transport promotes Smoothened cholesterylation at the endoplasmic reticulum的研究论文,揭示了GRAMD/ASTER家族蛋白介导质膜胆固醇运输进而调控内质网上SMO蛋白胆固醇化修饰的机制。

Hedgehog(Hh)信号通路对于胚胎发育及成体损伤组织、器官修复具有重要作用。在成年人中异常激活Hh信号通路与各种癌症的发生密切相关。Hh信号转导主要步骤包括:成熟形式的Hh蛋白与细胞质膜(PM)上的配体Ptched1(PTCH1)结合,解除PTCH1对Smoothened(SMO)的抑制,激活的SMO被转运到初级纤毛进而开启信号通路。
2017年4月,武汉大学生命科学学院宋保亮教授团队在Molecular Cell上首次报道了SMO蛋白第95位天冬氨酸(D95)可被胆固醇共价修饰。这一修饰对SMO参与Hh信号转导至关重要,在小鼠中将SMO胆固醇修饰位点突变导致胚胎致死【1】。因此SMO是否被胆固醇化修饰是Hh信号传递的一个关键节点。
2022年2月,该合作团队在《细胞研究》上报道了在钙离子存在时,SMO胆固醇化修饰由自催化完成;Hh可以激活STIM-ORAI1钙离子通道,导致早期胞内体中钙离子含量增加,进而增加早期胞内体上SMO的胆固醇化修饰【2】。
内质网(ER)作为蛋白质初始合成场所,对于ER上SMO胆固醇化修饰的调控尚不清楚。ER中胆固醇含量低而钙离子含量丰富。当质膜(PM)游离胆固醇含量增加时,GRAMD家族蛋白可以被招募到ER-PM接触位点,进而将PM上游离胆固醇转运到ER【3】。
本研究发现:当用Hh蛋白处理细胞后,GRAMD可以被招募到ER-PM接触位点,并将PM上游离的胆固醇转运到ER,进而增加ER上SMO的胆固醇化修饰。胆固醇化修饰后导致SMO构象发生变化,使SMO蛋白C末端的基序(RRxWxR)暴露,COPII蛋白复合体识别并结合该基序将SMO转运至高尔基体,在高尔基体上SMO完成糖基化修饰,成熟形式的SMO进入初级纤毛,开启信号通路(图1)。本研究将细胞内胆固醇转运与Hh信号转导联系起来,为深入研究Hh信号通路提供了新的方向。
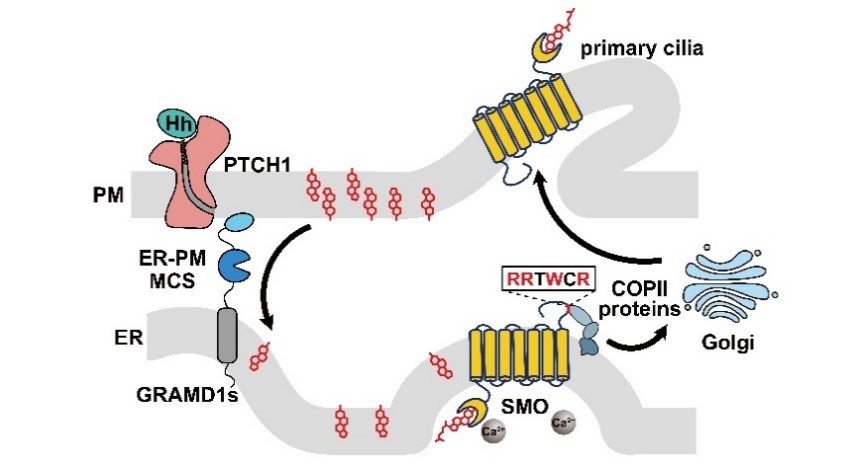
图1:Hh/PTCH1通过SMO调控信号通路的机制
武汉大学生命科学学院邱智萍博士和林子存博士为本论文共同第一作者。宋保亮院士为通讯作者。该工作得到国家自然科学基金委,武汉大学的资助,宋保亮获腾讯科学探索奖资助。
原文链接:
https://www.embopress.org/doi/full/10.15252/embj.2022111513
参考文献
1. Xiao X, et al. (2017) Cholesterol Modification of Smoothened Is Required for Hedgehog Signaling. Molecular cell 66(1):154-162 e110.
2. Hu A, et al. (2022) Cholesterylation of Smoothened is a calcium-accelerated autoreaction involving an intramolecular ester intermediate. Cell research.
3. Sandhu J, et al. (2018) Aster Proteins Facilitate Nonvesicular Plasma Membrane to ER Cholesterol Transport in Mammalian Cells. Cell 175(2):514-529 e520.